實例:
60℃時,分别向盛有10g水的A、B兩支試管中,加入等質量的甲、乙兩種固體
物質,使其充分溶解,溶解後的現象如圖1,圖二則是兩種物質的溶解度曲線。
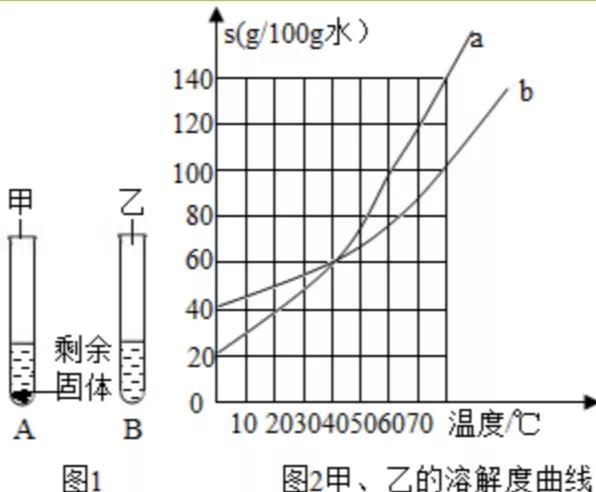
根據圖一圖二,下列選項錯誤的是
A、60℃時,B試管中的溶液可能是不飽和溶液。
B、圖1中A試管中剩餘物質可采用加水或加熱的方法讓其繼續溶解
C:根據圖1現象可知,圖2中b表示乙物質的溶解度曲線
D、測得a曲線表示的物質溶液的質量分數為37.5%,則在40℃時該溶液是飽和溶液!
難點解析:
根據AB試管的溶解現象,60°時甲有剩餘,而乙完全溶解,說明在這一溫度下乙的溶解度>甲的溶解度,所以圖2中a表示乙的溶解度曲線,b表示甲的溶解度曲線,并且在這一溫度下,A試管為飽和溶液,B試管可能是飽和溶液或者不飽和溶液(乙正好完全溶解則為飽和溶液,如果乙量不足,則是不飽和溶液)
由于甲物質的溶解度随着溫度的升高而增大,如果使剩餘的甲物質繼續溶解可以升高溶液的溫度,或者增加溶劑的量使其繼續溶解,根據圖二可知在40°時物質的溶解度是60g,所以此時溶液中溶質的質量分數是60÷(60 100)×100%=37.5%,所以此時溶液是飽和溶液
所以隻有C答案錯誤
重點知識:
溶解度曲線表示同種物質的溶解度與溫度變化的關系,曲線上的點都代表在此溫度下溶液為飽和溶液,曲線下面的點則表示為不飽和溶液,曲線上面的點表示物質有剩餘,但溶液為飽和溶液,
物質的溶解度隻與溫度有關,大多數固體物質的溶解度都随溫度的升高而增大;氫氧化鈣的溶解度随溫度的升高而溶解度降低,所有的氣體物質的溶解度随溫度的升高而降低,個别物質的溶解度與溫度變化相差不大如:NaCl
對溶解度随溫度升高而增大的固體物質,升高溫度飽和溶液變為不飽和容易,降低溫度後溶質有析出,此時溶液仍為飽和溶液
對溶解度随溫度升高而降低的固體物質,降低溫度飽和溶液變為不飽和容易,升高溫度後溶質有析出,此時溶液仍為飽和溶液。對溶解度相差較大的物質,可以通過升溫或者降溫的方式,使其中一種物質析出從而可以達到分離兩種物質的目的。
同學們都懂了嗎?不懂得同學和家長可以留言一起探讨學習!
,更多精彩资讯请关注tft每日頭條,我们将持续为您更新最新资讯!




